Servizi Aggiuntivi


- RISORSE
Hub di conoscenze Lionbridge
- Leadership di pensiero nell'AI
- Risultati positivi per i pazienti

Framework TRUST di Lionbridge
Rafforzare la fiducia nell'uso dell'intelligenza artificiale


Collaboratori internazionali: Allie Fritz
Director of Interpretations di Lionbridge

SELEZIONATE LA LINGUA:
I professionisti che si occupano dei processi di procurement e outsourcing in ambito clinico sono sottoposti a una crescente pressione per implementare soluzioni di intelligenza artificiale in grado di generare risparmi significativi, migliorare l'efficienza operativa e offrire maggiore controllo sui costi dei trial clinici. Gli studi di ricerca clinica sono notoriamente costosi. I costi medi di R&S nella fase pre-lancio di un nuovo farmaco variano da 161 milioni a 4,54 miliardi di dollari, a seconda dell'area terapeutica. Il mercato totale dei servizi linguistici per il settore Life Science in ambito clinico è stato stimato a 1,01 miliardi di dollari nel 2019 e il mercato globale potenziale per servizi linguistici e tecnologia nel 2023 ha raggiunto 2,68 miliardi di dollari.
Una volta che un candidato farmaco supera con successo la fase 1 degli studi sull'uomo, lo sviluppo clinico diventa multinazionale e richiede servizi linguistici e di localizzazione estesi per supportare i piani di sviluppo clinico globale. Tuttavia, gli sponsor sono spesso riluttanti ad adottare l'AI per i trial clinici e i risultati linguistici della ricerca, nonostante l'intelligenza artificiale stia già rivoluzionando diversi aspetti dei trial:
- Design
- Condotta
- Analisi
Lionbridge è fermamente convinta che le riforme dell'UE in materia di richieste di trial clinici rappresentino un caso ideale per l'uso dell'AI nel settore Life Science, in particolare per supportare le attività linguistiche e promuovere partnership strategiche con fornitori di servizi di traduzione per il settore Life Science.
Dossier di presentazione centralizzati in tutta l'UE: una nuova opportunità
L'implementazione del Sistema Informativo sulle Sperimentazioni Cliniche (CTIS) nell'UE consente agli sponsor dei trial clinici e ai produttori di dispositivi medici di presentare un unico dossier di richiesta di sperimentazione clinica per gli studi multinazionali condotti nell'UE. I regolamenti UE (CTR, MDR e IVDR) e la piattaforma CTIS facilitano un processo di autorizzazione congiunto in tutti gli Stati membri dell'UE.
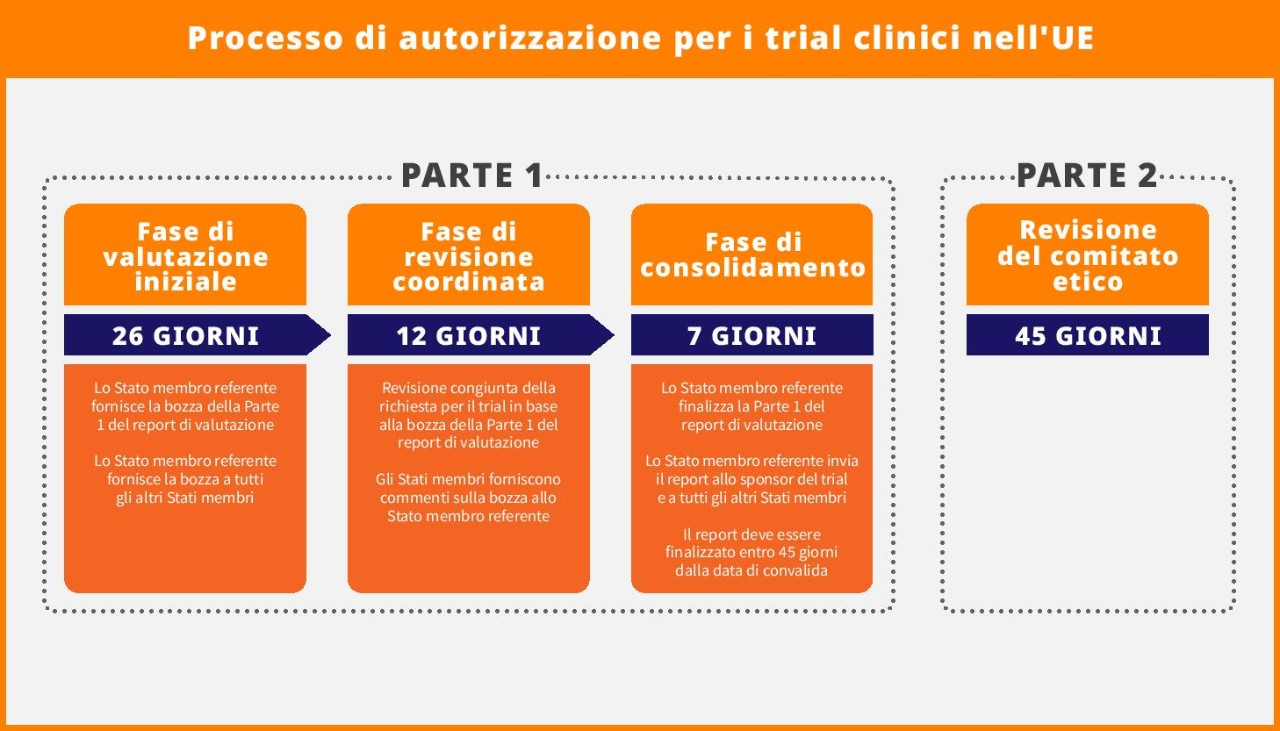
The clinical trial authorization process is streamlined into a 45-day procedure, with one Member State acting as the Reporting Member State (RMS) and responsible for coordinated assessment across all concerned Member States. Questo processo riduce la procedura di 15 giorni, rispetto al precedente processo di 60 giorni. Comprende questi passaggi sequenziali:
- Fase di valutazione di 26 giorni
- Fase di revisione coordinata di 12 giorni
- Fase di consolidamento di 7 giorni
Parallelamente, durante la stessa finestra di valutazione di 45 giorni, i Comitati etici di ogni Stato membro esaminano la Parte 2 del dossier di candidatura.
I risultati linguistici durante le fasi di revisione coordinata e consolidamento possono richiedere una rapida revisione oppure le autorità di regolamentazione possono richiedere informazioni aggiuntive nelle lingue locali. Il team del trial deve rispondere rapidamente alle richieste di informazioni da parte dell'autorità di regolamentazione e gestire rapidamente le attività linguistiche in tutti i Paesi, per evitare ritardi o decadenze automatiche delle richieste.
Centralizzazione dei i servizi linguistici: un imperativo strategico per l'intelligenza artificiale nei trial clinici
Le rigide tempistiche e i principi di decisione tacita dei regolamenti UE rivisti dovrebbero incoraggiare gli sponsor a centralizzare i servizi di traduzione dei trial clinici. La gestione dei risultati linguistici attraverso funzioni decentralizzate di gestione dei trial locali contraddice gli sforzi dei regolatori di armonizzare e snellire le procedure di autorizzazione dei trial clinici. Con numerosi studi registrativi svolti in diversi paesi dell'UE, la decentralizzazione può diventare un fattore di rischio per il raggiungimento dei traguardi critici della fase 3. Inoltre, adottando una strategia di procurement multi-fornitore, gli sponsor dei trial rischiano di perdere i risparmi significativi sui costi derivanti dall'uso di un unico sistema di AI e di servizi di traduzione tramite AI per i trial clinici, tra cui:
- Scalabilità centralizzata delle traduzioni
- Riepilogo
- Creazione di contenuti
Le strategie di procurement multivendor, spesso dettate dai Sistemi di Gestione della Qualità, aiutano a garantire la mitigazione dei rischi aziendali e a ottenere prezzi competitivi. Tuttavia, procurarsi i risultati linguistici da diversi fornitori di servizi linguistici all'interno dello stesso programma di sviluppo clinico è sconsiderato e probabilmente più rischioso di un approccio centralizzato. Seguire procedure QMS multivendor spesso porta a incoerenze e appesantisce i bilanci dei trial clinici. Questo è particolarmente gravoso in un'industria che controlla pesantemente i costi di R&S.
Gli sponsor possono usare l'AI per i trial clinici per ottenere risparmi incrementali sui costi, migliorando al contempo la qualità e la coerenza linguistica. Questo obiettivo può essere implementato a uno qualsiasi di questi livelli:
- Trial
- Composto
- Area terapeutica
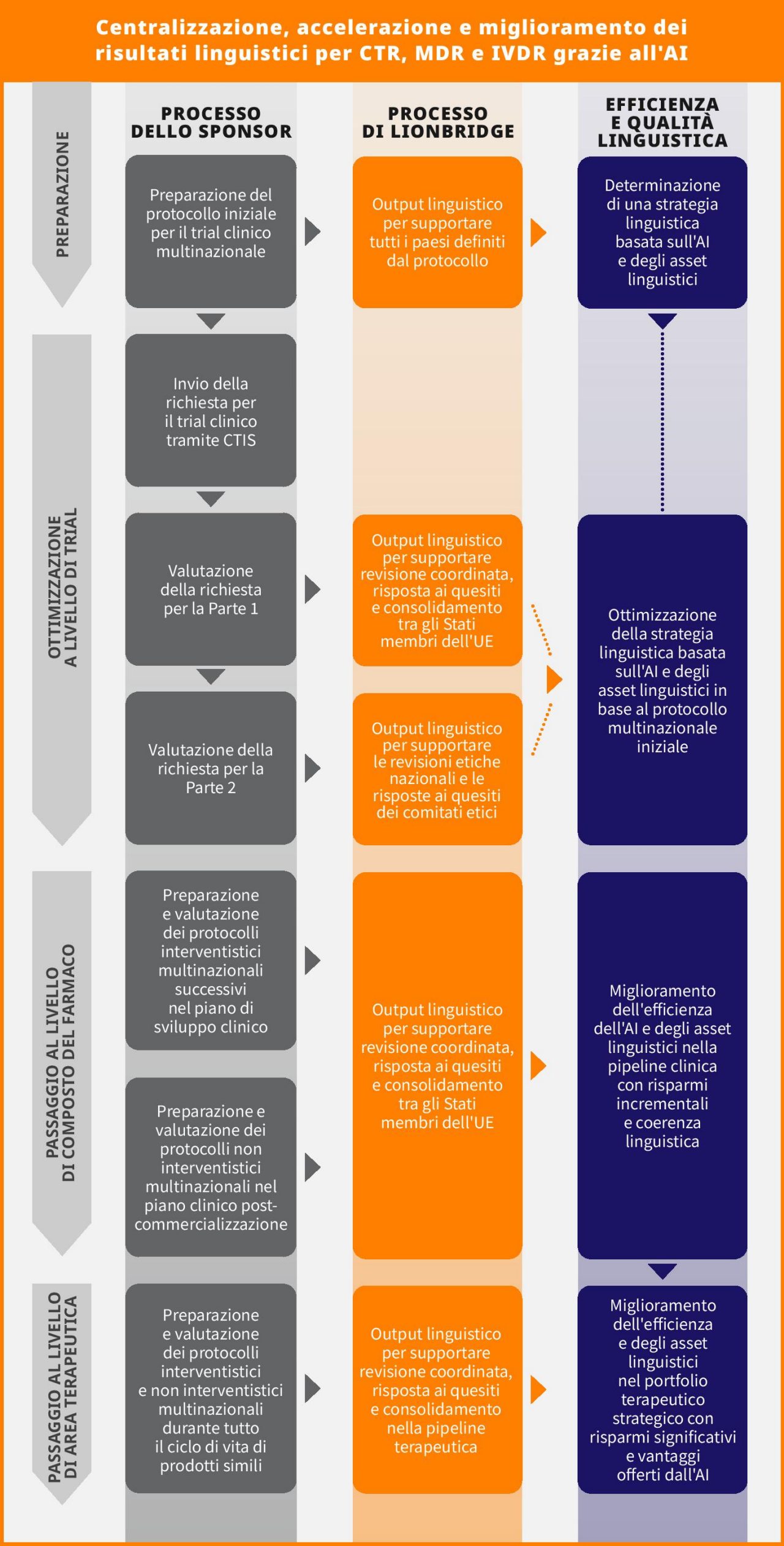
Centralizzazione dei risultati linguistici per gli studi combinati farmaco-dispositivo
I risultati linguistici supportati dall'AI non hanno solo un potenziale a livello di prodotto. I trial clinici combinano sempre più spesso l'indagine su un medicinale con lo studio delle prestazioni di un dispositivo diagnostico in vitro o un'indagine clinica su un dispositivo medico.
Sebbene sia stata identificata una mancanza di allineamento nel processo di autorizzazione dei trial clinici tra CTR, MDR e IVDR, un approccio centralizzato per quanto riguarda l'output linguistico può anche favorire un miglioramento dell'efficienza degli studi di combinazione. Lionbridge raccomanda di utilizzare l'AI per la strategia linguistica dei trial clinici attraverso i tipi di contenuto per gli studi combinati. Le terminologie, le risorse linguistiche e i contenuti possono essere condivisi tra un dispositivo diagnostico in vitro e un farmaco, per supportare lo sviluppo di una medicina personalizzata. Durante lo sviluppo del farmaco e della sua diagnostica complementare, i flussi di lavoro dell'AI possono essere predefiniti e implementati insieme ai glossari. Ciò contribuisce a:
- Migliorare l'efficienza
- Modificare le procedure
- Allineare le comunicazioni e le affermazioni relative alle prestazioni per supportare obiettivi condivisi
Trattate il vostro fornitore di servizi linguistici come una CRO
Con l'aumento dei costi della ricerca clinica, le Organizzazioni di Ricerca a Contratto (CRO) sono diventate essenziali per l'esecuzione di trial clinici efficienti e di successo. Nel tempo, il loro ruolo si è evoluto da fornitori di servizi incaricati delle attività amministrative dei trial a veri e propri partner che hanno un ruolo attivo per quanto riguarda:
- Progettazione del trial
- Gestione dei dati
- Reclutamento dei pazienti
La digitalizzazione e l'intelligenza artificiale per i trial clinici hanno anche aperto nuove strade per le partnership strategiche nella relazione B2B.
Grazie ai Large Language Model (LLM) che trasformano l'intero percorso dei contenuti, gli sponsor oggi possono instaurare partnership strategiche simili con i fornitori di servizi linguistici e sfruttare appieno i vantaggi offerti dall'intelligenza artificiale per i trial clinici.
Contattateci.
Siete pronti a esplorare le soluzioni linguistiche e di contenuti per supportare l'intero ciclo di vita dello sviluppo di farmaci e dispositivi medici? Lionbridge offre un'esperienza multidisciplinare unica con LLM, eccellenza linguistica, normative e contenuti del settore Life Science. Offriamo soluzioni AI avanzate e su misura, dalla pianificazione alla creazione, all'analisi, alla sintesi e alla localizzazione. Contattateci.


