

- 資源


全球各地的採購與臨床委外專業人士無不面臨一個日漸高漲的壓力:實作 AI 解決方案以便大幅降低成本、提高營運效率,以及更妥善地監督臨床試驗的成本。臨床研究試驗的成本是出了名的高。想要推出新藥,上市前的研發 (R&D) 成本大概就要 1.61 億美元到 45.4 億美元 (視治療領域而定)。截至 2019 年,臨床生命科學領域中語言服務市場的總值估計為 10.1 億美元,而 2023 年語言服務與技術的全球整體潛在市場總值估計更有 26.8 億美元之多。
一旦候選藥物成功通過第一期人體試驗,臨床開發將會轉為跨國進行,因此也會有大量的語言服務與本地化工作,好支援全球臨床開發計畫。然而,出於風險考量,委託者往往對在臨床試驗和研究語言結果中應用 AI 持保守態度 — 即使 AI 早已徹底改變了試驗的以下方面:
- 設計
- 執行
- 分析
Lionbridge 深信歐盟在臨床試驗申請上的改革,恰好就是 AI 生命科學應用的典型案例,尤其有利於支援語言結果,以及與生命科學翻譯服務供應商建立策略採購合作關係。
跨歐盟地區的集中化送件:新商機
歐盟實作臨床試驗資訊系統 (Clinical Trials Information System,CTIS) 後,在歐盟執行跨國研究的臨床試驗委託者及醫療器材製造商,現在只需要提交一次臨床試驗申請文件即可。透過歐盟法規 (CTR、MDR 和 IVDR) 搭配 CTIS 平台這種雙管齊下的做法,會更有益於增進所有歐盟成員國聯合授權流程的效率。
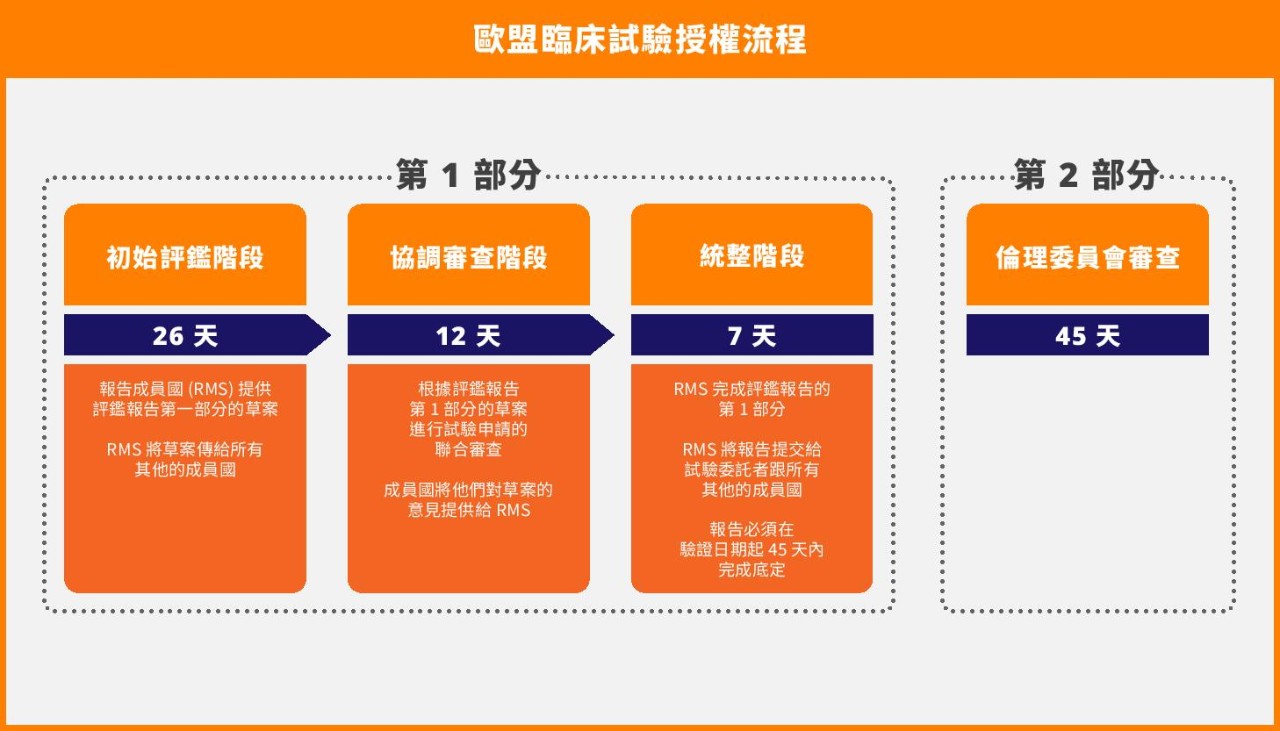
臨床試驗授權流程現已簡化成為期 45 天的程序,其中一個成員國會擔任「報告成員國」(Reporting Member State,RMS),負責協調所有相關成員國的評鑑事宜。這個程序比之前 60 天的程序少了 15 天,它是依序進行包括以下這些步驟:
- 26 天的評鑑階段
- 12 天的協調審查階段
- 7 天的統整階段
與此同時,各個成員國的倫理委員會也會在這個 45 天的時程內,審理申請文件的第 2 部分 (Part 2)。
在協調審閱以及統整的階段,語言結果可能會需要快速地加以修訂,監管機關也可能會要求以在地語言提供更多資訊。試驗團隊必須要能迅速回應監管機關的資訊補件要求 (Request for Information),並快捷地管理所有國家/地區的語言活動,以避免延宕或申請自動失效。
語言服務集中化:臨床試驗適用之 AI 的策略性必備條件
修訂後的歐盟法規有著嚴格的時程規定以及默示的決策原則,這些或許都會激勵委託者將臨床試驗翻譯服務集中化。因為監管機關均致力調和與簡化臨床試驗授權程序,因此以分散式的在地試驗管理單位來管理語言結果這種做法,可說是與監管機關背道而馳。許多樞紐性研究都是跨多個歐盟國家執行,分散式的去中心化做法,反而會變成有礙達成關鍵性第 3 期里程碑的一個風險因子。此外,試驗委託者若仍堅持採用多供應商採購策略,可能會因此錯失在臨床試驗中使用單一 AI 系統及 AI 翻譯所能節省的大幅成本,包括:
- 集中化的翻譯範疇擴增
- 總結
- 內容創作
多供應商採購策略往往是由品質管理系統所主導,這些策略有助確保降低業務風險並取得具競爭優勢的價格。然而,在同一個臨床開發方案中向不同的語言服務供應商採購語言結果,不但不明智,甚至可以說比起集中化的做法風險更高。採用多供應商的 QMS 程序,經常會造成不一致的問題,亦會增加臨床試驗預算的負擔。對一個研發 (R&D) 成本受到高度審查的產業來說,這尤其麻煩。
試驗委託者可以採用臨床試驗適用的 AI 來逐步節省成本,同時亦有助於改善語言品質與一致性。這樣的目標可以在以下任一個層級實行:
- 試驗
- 化合物
- 治療
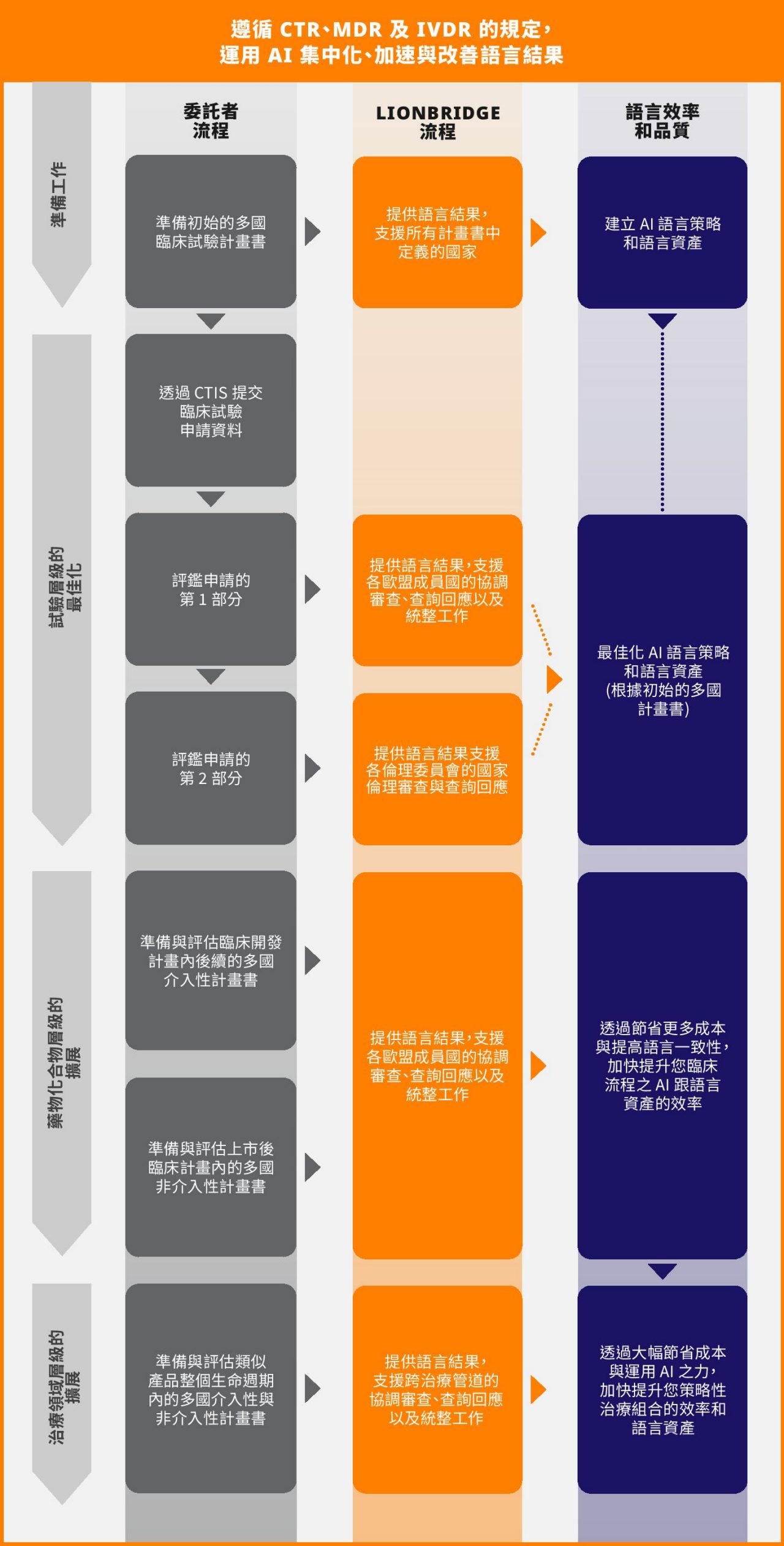
複合式藥物/器材研究的語言結果集中化
採用 AI 技術支援的語言結果,也能在產品層級之外發揮很大的潛力。臨床試驗正越來越傾向將藥品的研究,與體外診斷醫療器材的成效研究或醫療器材的臨床研究相結合。
雖然業界已發現 CTR、MDR 和 IVDR 彼此的臨床試驗授權流程存在著不一致的問題,但以集中化的做法來處理語言結果,應該會有助於提高複合式研究的效率。Lionbridge 建議複合式研究可以將 AI 納入臨床試驗的語言策略,以便應用於不同的內容類型。例如,對於體外診斷醫療器材結合藥物的複合式研究,便可跨不同研究分享術語、語言資產及內容,以支援個人化的藥物開發。在藥物及其伴同性診斷的開發階段,也可預先定義好 AI 工作流程並與詞彙表一併實作,進而有益於:
- 推動效率
- 變更程序
- 製作一致的訊息與成效聲明,以互相支持彼此的評估指標
將您的語言服務供應商視為是 CRO
隨著臨床研究的成本日漸增加,委託研究機構 (Contract Research Organization,CRO) 已成為成功且有效率執行臨床試驗的必要條件。隨著時間演進,他們的角色也從承接試驗行政管理職責的服務供應商,變成了會影響以下事項的真正合作夥伴:
- 試驗設計
- 資料管理
- 病人招募
數位試驗執行與臨床試驗適用的 AI,也為 B2B 往來的策略合作開拓了新的途徑。
有鑑於大型語言模型 (LLM) 徹底改變了內容歷程的整個面貌,委託者現在亦可跟語言服務供應商 (LSP) 結成類似的策略合作關係,進而充分獲益於臨床試驗適用的 AI。
與我們聯絡
準備好探索語言和內容解決方案,了解它們如何能支援您藥物與醫療器材的整個開發生命週期嗎?無論是 LLM、語言卓越能力、法規還是生命科學內容,Lionbridge 具備獨樹一格的跨領域專業能力,能提供先進且量身客製的 AI 解決方案,協助您處理規劃、製作、分析、總結、本地化等眾多事務。歡迎與我們聯絡。




