사람의 전문성과 강력한 AI의 융합
Lionbridge Aurora AI™는 다국어 콘텐츠를 강화하고, 관련성과 개인화된 콘텐츠로 잠재고객을 확장하는 AI 기반 글로벌 플랫폼입니다.

- 리소스


제약 업계 경험이 있는 사람이라면 규제 프로세스가 간단하다고 감히 말할 수 없을 것입니다.
현재 임상 연구 환경은 놀라울 정도로 방대하며 전 세계에서 매년 진행하는 임상시험 횟수도 계속 증가하고 있습니다. 현재 전 세계 204개국에서 284,522개의 연구가 진행 중입니다. 이 규모는 흥미를 자아냅니다. 더 많은 혁신은 더 많은 인구의 더 많은 질병에 대한 솔루션을 제공합니다. 하지만 이미 복잡한 시장을 더욱 복잡하게 만들기도 합니다.
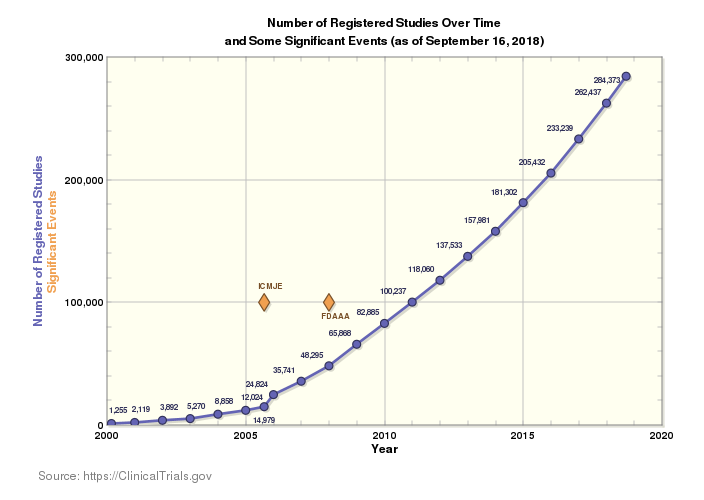
더 많은 국가에서 더 많은 언어로 임상시험이 진행 중이라는 뜻은 더 많은 규칙을 따르고, 더 많은 사람을 고려해야 하며, 임상 공급망 추적에 더 많은 규제를 따라야 한다는 것을 의미합니다. 이런 상황은 시장에 빠르게 출시하고, 비용을 줄이며, 공급 및 납품 과정의 실수를 줄여야 한다는 당연한 압박과 함께 복잡한 규정을 준수하는 일을 더 어렵게 만듭니다.
'규정 준수'가 반드시 '복잡함'을 의미할까요? 그렇지 않습니다. 똑똑한 기업이 임상 라벨링 프로세스를 간소화하는 세 가지 방법을 소개합니다.
1. 번역 및 규제 대상 콘텐츠 관련 인증 데이터베이스를 만든다.
정확성과 규정 준수를 보장하는 임상 라벨 준비 프로세스는 대부분 수동으로 이뤄집니다. 여러 관계자가 출력 전 서류를 검토해야 하며, 여러 공급업체의 의견 및 관점이 다를 것이며, 다양한 이해 당사자들의 번역 선호도도 다를 것입니다. 이것이 제약 회사가 새 임상 라벨링 계획을 세울 때마다 '처음부터' 다시 시작하게 되는 이유입니다.
일관되고 종합적인 문구 라이브러리와 함께 번역 및 규제 대상 콘텐츠 관련 인증 데이터베이스가 있다면 일정 단축, 콘텐츠 표준화, 최종 단계에서의 신속한 변경 등이 가능하며, 글로벌 프로세스의 일관성 유지에 따른 위험도 줄일 수 있습니다. 즉, 제품이 더 빨리, 더 저렴하게, 그리고 더 적게 노출된 상태로 시장에 출시될 수 있습니다.
2. 동료가 아닌 전담 현지 전문가에게 의지한다.
제약 회사는 적은 리소스로 더 많은 성과를 얻어내기 위해 분투하며, '대여한 리소스'로 내부에서 규제를 관리하며 비용을 줄이기 위해 노력할 때가 많습니다. 하지만 규정을 지키며 임상 라벨 프로세스를 완료하기 위해 동료의 힘을 빌렸을 때는 실제로 비용 및 복잡성이 더 커지는 경우가 많습니다. 왜 그럴까요? '라벨마다' 규제 확인 및 번역 프로세스를 거치기 때문에 소요 시간이 길어지고, 오류 발생률이 높아지며, 규정 준수 여부를 추적하기가 더 어려워지기 때문입니다.
똑똑한 조직이라면 규제 및 언어 전문성을 지닌 현지 전문가에게 투자하는 것이 늘 정확하고 빠른 라벨을 전달하는 확실한 방법이라는 것을 알고 있습니다. '라벨마다' 새로운 접근법을 사용하지 않고 전문가와 함께 프로세스를 표준화함으로써 위험 요소를 낮출 수 있습니다.
3. 조절 가능한 창의력을 수용한다.
갈수록 복잡해지고 변화무쌍한 규제 환경으로 인한 문제를 해결하는 가장 좋은 방법은 약간의 창의력을 발휘하는 것입니다. 예를 들어 라벨링 프로세스를 의도적으로 늦게 시작함으로써 편집 및 재라벨링 횟수를 줄일 수 있고, 보관 및 운송, 유통 기한 관리에도 도움이 될 수 있습니다. 또한 풍부한 문구 라이브러리와 혁신적인 언어 기술을 사용해 번역 속도를 높일 수도 있습니다.
하지만 복잡성을 줄이기 위한 이런 솔루션은 역설적으로 또 다른 복잡함을 낳을 수 있습니다. 각 솔루션마다 특별한 계획과 개발, 관리가 필요하기 때문입니다. 따라서 이러한 문제를 종합적이고 체계적이며 창의적으로 해결하고 싶다면 이런 실행 전략을 자유자재로 다룰 수 있는 파트너와 함께 하는 것이 최선입니다.
Lionbridge 생명과학에서는 고객이 더욱 안전하고, 효과적이며, 합리적인 비용의 약물을 시장에 빠르게 출시하기 위한 솔루션을 꾸준히 찾고 있습니다. 이런 문제를 어떻게 해결할 수 있는지, 그리고 날로 복잡해지는 IMP 및 IND와 관련한 임상 라벨링 문제를 동료들이 어떻게 처리하고 있는지 궁금하다면 DIA에서 Lionbridge 생명과학 VP Peter Quigley의 최근 웨비나를 시청하거나 Lionbridge에 지금 문의하세요.