


人間の専門知識と強力な AI 機能の融合
Lionbridge Aurora AI™ は、AI主導のグローバルコンテンツプラットフォームで、多言語コンテンツを強化し、関連性の高いパーソナライズされたコンテンツでオーディエンスを拡大します。

- リソース


製薬業界での勤務経験があれば、規制プロセスは簡単であると敢えて言う人はいないでしょう。
現在、臨床研究のすそ野は非常に広大で、世界中で行われている試験の数も年々増加しています。現在、世界の 204 か国で 284,522 件の研究が行われています。この規模には胸が躍ります。より多くのイノベーションによって、より多くの患者に向けて、より多くの疾患に対するソリューションがもたらされるのです。しかしこれはまた、すでに込み入った市場の複雑さをさらに高めることにもつながります。
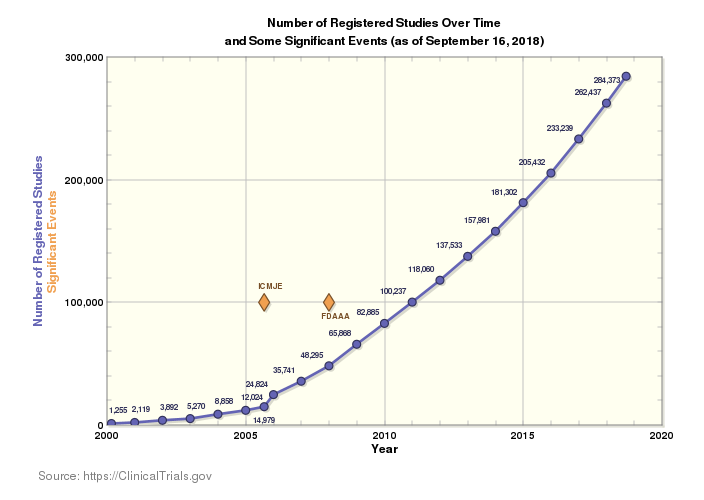
より多くの国々、より多くの言語で、さらに多くの試験を行うことは、従うべき規則、考慮すべき人々、臨床サプライチェーンで追跡すべき規制が増えることになります。これが、市場投入までの時間短縮、コスト削減、供給と配送のエラーをなくすという絶え間ない圧力と相まって、規制への準拠をこれまで以上に複雑にしています。
「規制への準拠」が「複雑」である必要があるのでしょうか? そうではありません。臨床ラベリングの複雑さを賢明な企業がどのように軽減しているか、その 3 つの方法を以下にご紹介します。
1.翻訳および規制コンテンツ用の認定データベースを作成する。
規制への準拠と精度の両方を確保する点で、臨床ラベルを準備するプロセスは主に手作業で行われています。書類を提出するまでに複数の担当者が確認する必要があり、多数のベンダーが異なる意見や見解を持ち、さまざまな関係者が翻訳に対して多様な好みを持っています。そのため、製薬会社は新しい臨床ラベル作成に取り組むたびに、「一からやり直さなければならない」場合があります。
一貫性のある包括的な語句のライブラリーを備えた、翻訳および規制コンテンツ用の認定データベースがあれば、グローバルなプロセス全体で一貫性を維持し、それにより、サイクルタイムの短縮、コンテンツの標準化、後期段階での迅速な変更が可能になり、リスクが軽減されます。その結果、製品をより迅速かつ安価に、よりリスクを抑えて市場に出すことができます。
2.同僚ではなく、対象国内の専門家を頼りにする。
製薬会社は、より少ないリソースでより多くのことを行おうとしているため、コストを抑え、「借りてきたリソース」を使って社内で規制管理をすることがよくあります。しかし、規制への準拠を同僚に頼り、臨床ラベリングのプロセスを完了しようとすると、コストも複雑さも増すことが多いのが実情です。それはなぜでしょうか? 「ラベルごと」に規制の検証と翻訳を行うプロセスにより、リード タイムが長くなってエラーの発生率が高くなり、コンプライアンスの追跡が難しくなるからです。
賢明な組織は、規制と言語の両方の専門知識を持つ対象国内の適格な専門家に投資することで、ラベリングを毎回正確かつ迅速に行うことを確保しています。また、「ラベルごと」の方法から離れ、これらの専門家が関連するプロセスを標準化することにより、リスク プロファイルも低下させています。
3.管理された創造力を受け入れる。
複雑さの増大と規制環境の変化によって生じる問題に対する最善の解決策を生み出すには、ほんの少しの創造力が必要になります。たとえば、ラベリングのプロセスを意図的に遅く始めることで、編集や再ラベリングの回数を最小限に抑えることができます。これは、ストレージ、ロジスティクス、保存期間の管理にも役立ちます。または、堅実かつ豊富な語句のライブラリーと革新的な言語技術を使用すれば、翻訳を迅速化できます。
しかし逆説的に、複雑さを軽減しようとすると、これらの解決策によって新たな混乱が生じる可能性もあります。それぞれに専門的な設計、開発、および管理が必要です。問題を包括的かつ体系的、創造的に解決したいのであれば、これらのロジスティクスを処理できるパートナーと協働することが最善の方法です。
ライオンブリッジ ライフ サイエンス部門では、お客様が安全かつ効果的に、手頃な価格の医薬品を可能な限り短期間で市場に投入しようとする取り組みを阻害する各種問題の解決策を常に模索しています。これらの問題を克服する方法と、ますます複雑さを増す IMP および IND の臨床ラベリングに対する他の企業の対処方法について詳しくお知りになりたい方は、DIA のライオンブリッジのライフ サイエンス部門の担当 VP、ピーター キグリーによる最新ウェビナーをご覧いただくか、当社までお問い合わせください。
#ライフ サイエンス #臨床研究 #臨床試験 #臨床試験のラベリング #製薬会社 #規制コンテンツ




