Exklusivitet genom innovation: AI-baserade eLearning-lösningar för detaljhandel och lyxvaror


Fallstudie: Flerspråkiga kampanjer i detaljhandeln
Nya AI-baserade lösningar för skapande av innehåll hos stort sport- och klädföretag


Mänsklig expertis och kraftfull AI hand i hand
Lionbridge Aurora AI™ är en global AI‑plattform som stärker flerspråkigt innehåll och utökar publiken med relevant, anpassat innehåll.

- RESURSER


Ingen med erfarenhet från läkemedelsindustrin skulle ens antyda att regleringsprocessen är enkel.
Ta reda på hur du kan minska komplexiteten.
Det nuvarande kliniska forskningslandskapet är otroligt stort och antalet prövningar som görs över hela världen ökar för varje år. För närvarande pågår 284 522 studier i 204 länder över hela världen. Denna omfattning är spännande – mer innovation ger fler lösningar för fler sjukdomar i fler populationer – men det för också med sig en ökad komplexitet till en redan komplicerad marknad.
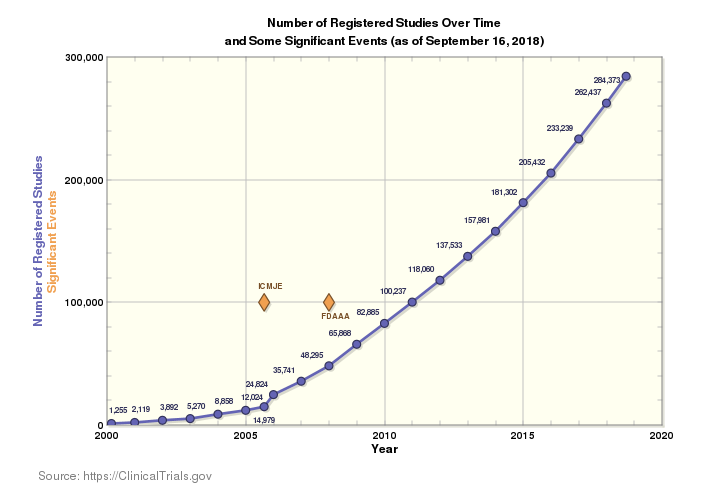
Fler prövningar i fler länder och på fler språk innebär fler regler att följa, fler människor att tänka på och fler regler att följa för kliniska leveranskedjor. Detta i kombination med de ständigt närvarande drivkrafterna att komma ut på marknaden snabbare, sänka kostnaderna och eliminera fel i leverans och utlämning gör det svårare än någonsin att säkerställa regelefterlevnad.
Måste ”korrekt” innebära ”komplicerat”? Nej. Här är tre sätt som smarta företag kan använda sig av för att minska komplexiteten i den kliniska märkningsprocessen.
1. Skapa en certifierad databas för översättning och regulatoriskt innehåll.
Processen med att framställa kliniska etiketter på ett sätt som säkerställer både noggrannhet och efterlevnad är till stor del manuell. Flera kontakter måste granska dokumentationen innan den går till produktion, många leverantörer har olika uppfattningar och perspektiv, och olika parter har olika preferenser när det gäller översättningar – vilket kan leda till att läkemedelsföretag återuppfinner hjulet varje gång de genomgår ett nytt initiativ för klinisk märkning.
Certifierade databaser för översättningar och regulatoriskt innehåll – med konsekventa och omfattande frasbibliotek – minskar cykeltiden, standardiserar innehållet, möjliggör snabbare ändringar i sena faser och minskar risken genom att vara konsekventa under hela din globala process. Sammanfattningsvis: Dina produkter når marknaden snabbare, billigare och med mindre utsatthet.
2. Förlita dig på inhemska experter – inte på dina kollegor.
Eftersom läkemedelsföretag strävar efter att göra mer med färre resurser försöker de ofta hålla kostnaderna nere genom att hantera förordningar internt med ”lånade resurser”. Men att luta dig mot dina kollegor för att följa och genomföra den kliniska märkningsprocessen ökar ofta faktiskt både kostnaderna och komplexiteten. Varför? Denna process för regulatorisk validering och översättning ”per etikett” ger längre ledtider, fler fel samt gör det svårare att spåra efterlevnaden.
Smarta organisationer vet att investeringar i rätt inhemska experter med både regulatorisk och språklig expertis säkerställer att deras märkning alltid levereras korrekt och snabbt. Och genom att gå ifrån metoden ”per etikett” och standardisera processen kring dessa experter sänker de riskprofilen.
3. Omfamna kontrollerad kreativitet.
Några av de bästa lösningarna på problemen som uppstår till följd av ökad komplexitet och ett förändrat regulatoriskt landskap kräver en del kreativitet. Till exempel kan ditt företag minimera antalet redigeringsrundor och ommärkning genom att få en avsiktligt sen start på märkningsprocessen, vilket också kan vara till hjälp när det kommer till lagring, logistik och hållbarhet. Eller så kan du påskynda översättningar med användning av stabila frasbibliotek och innovativ språkteknik.
Paradoxalt nog kan dessa lösningar, i ett försök att minska komplexiteten, göra det mer komplicerat. Var och en kräver design, utveckling och hantering av experter. Om du vill lösa dina problem heltäckande, systematiskt och kreativt vinner du oftast på att arbeta tillsammans med en partner som kan hantera detta åt dig.
På Lionbridge Life Sciences letar vi ständigt efter sätt att hjälpa våra kunder att övervinna de problem som hindrar dem från att få fram säkra, effektiva och prisvärda läkemedel till marknaden så snabbt som möjligt. Ta reda på mer om hur du kan lösa dessa problem och om vad dina kollegor gör för att hantera den allt större komplexiteten när det gäller klinisk märkning för IMP och IND genom att titta på detta webbinarium med Lionbridge Life Sciences VD, Peter Quigley, via DIA eller kontakta oss.