Esclusività in ogni dettaglio: soluzioni di eLearning basate sull'AI per il lusso e la vendita al dettaglio



Esperienza umana unita alla potenza dell'AI
Lionbridge Aurora AI™ è una piattaforma AI globale che potenzia i contenuti multilingue e amplia il pubblico con contenuti pertinenti e personalizzati.

- RISORSE
Hub di conoscenze Lionbridge
- Leadership di pensiero nell'AI
- Risultati positivi per i pazienti

Framework TRUST di Lionbridge
Rafforzare la fiducia nell'uso dell'intelligenza artificiale


Collaboratori internazionali: Allie Fritz
Director of Interpretations di Lionbridge

SELEZIONATE LA LINGUA:
Nessuno con una certa esperienza nel settore farmaceutico oserebbe avvalorare la semplicità del processo normativo.
Scoprite come ridurre la complessità.
L'attuale panorama della ricerca clinica è incredibilmente vasto e il numero di trial svolti nel mondo cresce ogni anno. Attualmente sono in corso 284.522 studi in 204 paesi del mondo. Questi numeri suscitano entusiasmo, in quanto più innovazione produce più soluzioni per più malattie in diverse popolazioni, ma introduce anche maggiore complessità in un mercato già intricato.
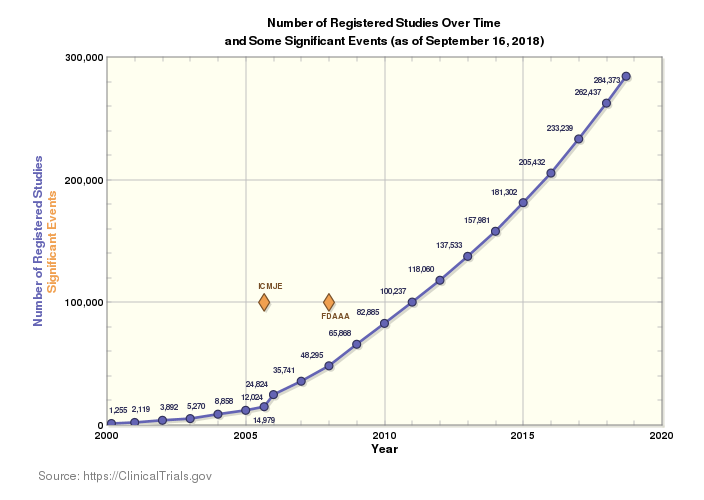
Più trial in più paesi e lingue significano più regole da seguire, più persone di cui tenere conto e più regolamenti di cui tenere traccia per le supply chain in ambito clinico. Tutto questo, associato alla pressante esigenza di ridurre il time-to market e i costi ed eliminare gli errori nell'erogazione e nella distribuzione, rende la conformità più complessa che mai.
Conformità significa necessariamente complessità? No. Ecco tre modi in cui le aziende più avvedute riducono la complessità del processo di creazione di etichette in ambito clinico.
1. Create un database certificato per le traduzioni e i contenuti normativi.
Il processo di preparazione delle etichette in ambito clinico in modo da garantire accuratezza e conformità è in gran parte manuale. Più contatti devono esaminare la documentazione prima che venga distribuita, diversi fornitori hanno opinioni e prospettive differenti e più parti hanno preferenze specifiche per la traduzione e tutto questo può costringere le case farmaceutiche a ricominciare da zero ogni volta che intraprendono una nuova iniziativa di creazione di etichette in ambito clinico.
Database certificati per traduzioni e contenuti normativi, con raccolte di frasi coerenti e complete, riducono i tempi, standardizzano i contenuti, permettono rapide modifiche nelle fasi finali e attenuano i rischi assicurando la coerenza lungo tutto il processo globale. Conclusione: i prodotti vengono introdotti nel mercato più rapidamente, a costi ridotti e con un'esposizione minore.
2. Affidatevi a esperti locali dedicati, non ai vostri colleghi.
Mentre lottano per fare sempre di più con meno risorse, le case farmaceutiche tentano spesso di tenere bassi i costi e di gestire le normative internamente con "risorse prese in prestito". Ma la pratica di affidarsi ai colleghi per la conformità e il completamento del processo di creazione di etichette in realtà spesso aumenta i costi e la complessità. Perché? Questo processo "etichetta per etichetta" per la convalida normativa e la traduzione implica tempi più prolungati, più errori e più difficoltà nel tenere traccia della conformità.
Le aziende più avvedute sanno che la ricerca di esperti locali competenti con esperienza sia linguistica sia normativa assicura un processo di creazione di etichette accurato e rapido ogni volta. E rinunciando a un approccio "etichetta per etichetta" e standardizzando il processo con il supporto di questi esperti, queste aziende riducono il proprio profilo di rischio.
3. Adottate un approccio creativo controllato.
Alcune delle migliori soluzioni ai problemi legati alla maggiore complessità e a un panorama normativo in continua trasformazione richiedono una certa creatività. Ad esempio, la vostra azienda potrebbe ridurre al minimo i cicli di modifiche e la creazione di nuove etichette assicurandosi un inizio intenzionalmente tardivo per il processo, che semplificherebbe anche la gestione di archiviazione, logistica e durata. Oppure potreste accelerare le traduzioni tramite solide raccolte di frasi e tecnologie linguistiche innovative.
Paradossalmente, tuttavia, nel tentativo di ridurre la complessità, queste soluzioni possono creare altre complicazioni. Ognuna richiede progettazione, sviluppo e gestione a cura di specialisti. Se volete risolvere i vostri problemi in modo completo, sistematicamente e creativamente, spesso la soluzione migliore è collaborare con un partner in grado di gestire questi aspetti logistici per voi.
Lionbridge Life Science è alla continua ricerca di nuovi modi per aiutare i nostri clienti a superare i problemi che impediscono di introdurre nel mercato farmaci sicuri, efficaci e convenienti il più rapidamente possibile. Scoprite come risolvere questi problemi e che cosa stanno facendo i vostri colleghi per affrontare con successo la sempre maggiore complessità della creazione di etichette in ambito clinico per prodotti IMP e IND guardando questo webinar recente con il Lionbridge Life Sciences VP Peter Quigley tramite DIA oppure contattateci.